Sistemas validados


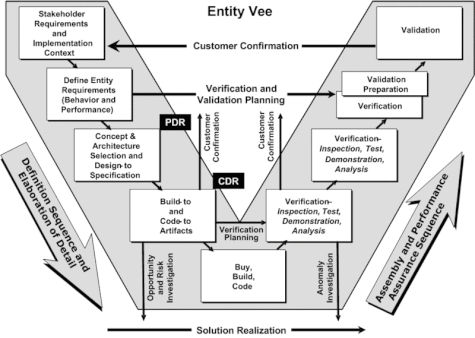
Con la necesidad actual de validar los sistemas bajo los requerimientos de la FDA "21CFR Part 11" y otros estándares, MIMCASI ayuda a sus clientes para que sus proyectos se lleven a cabo bajo el modelo "V Shape", generando junto con ellos los documentos necesarios desde la fase conceptual hasta la certificación.
De esta manera ayudamos al cliente a ahorrar dinero y tiempo al hacer una clara transferencia de la ingeniería a la validación. Preparamos con usted esta importante estafeta.
Juntos haremos de la pre-validación un pase rápido para concluir con un proyecto validado.
| Etapa | Actividades |
|
| Planeación |
Plan de proyecto Plan maestro de validación |
|
| Definición del sistema |
"User Requirement Specifications (USR)" Validación de riesgos |
|
| Diseño del sistema |
Especificaciones funcionales (FT) Especificaciones de diseño (DS) Revisión de diseño Requerimientos de "traceability" |
|
| Desarrollo |
Desarrollo del sistema Revisión del código fuente o programa Prueba del sistema "Standar Operation Procedures (SOP) |
|
| Verificación |
Installation Qualification (IQ)* Operational Qualification (OQ)** Performance Qualifacation (PQ)*** Qualification reports |
|
| Revisión |
Revisión de la calificación Revisión de la validación Certificado de liberación |